基因组所最新研究成果揭示肾癌发病机制
近日,基因组所基因组学与信息重点实验室刘江课题组与芝加哥大学的研究人员合作,在肾癌发病机制的研究中取得重要进展,揭示在低氧的生理条件下,核蛋白SPOP(speckle-type POZ protein) 的过表达和错误定位是引发肾癌产生的核心因素。相关学术论文“SPOP Promotes Tumorigenesis by Acting as a Key Regulatory Hub in Kidney Cancer”在Cancer Cell杂志上在线发表。
肾癌是泌尿生殖系常见恶性肿瘤之一,约占成人恶性肿瘤的3%左右,死亡率占癌症死亡的2%。目前肾癌最主要治疗方法是肾根治性手术切除,然而肾癌起病隐匿,往往缺乏早期临床表现。大约30%的肾癌患者在诊断时已经发生转移,未转移的肾癌患者在进行切除术后,还有大约40%的患者会复发。并且肾癌对放疗、化疗均不敏感。因此,急需深入探索肾癌发病的分子机制,找到肾癌早期诊断和治疗的分子靶标。
肾透明细胞癌是肾癌最常见的病理学类型,占肾癌的75%,SPOP是泛素连接酶E3 家族成员Cul3 与底物结合的桥梁蛋白(adaptor),通过介导许多核蛋白的泛素化而促进它们的降解,从而参与调控细胞的多种功能。刘江博士过去的研究发现,SPOP在99%的肾透明细胞癌的肿瘤组织中过表达,而在对应的正常肾组织中表达很低,还发现转移性肾透明细胞癌SPOP仍过表达,阐明SPOP是透明细胞癌的标记分子(Science,2009)。
课题组近期的研究结果显示,核蛋白SPOP 在肾癌组织中过量表达并错误定位在细胞质里。肾癌中,过度活化的缺氧诱导因子HIF可以转录调控SPOP表达。低氧微环境可以驱使过表达的SPOP蛋白在肾癌细胞质中大量累积。与核定位SPOP 的促凋亡功能不同,胞质型SPOP 能加速细胞增殖。通过生物信息分析和实验验证,发现胞质中的SPOP与肿瘤抑制因子PTEN 和ERK 磷酸酶DUSP7 相结合,并通过泛素化通路使其降解,从而激活了PI3K-Akt和ERK信号通路。此外,肾癌中SPOP还通过降解Daxx和Gli2来抑制细胞凋亡和促进细胞增殖,从而导致肿瘤产生。相反敲除SPOP后能特异性杀死肾透明细胞癌,但对正常细胞影响较小。
以上结果阐明了SPOP在促进肾癌形成中的重要机制,即作为一个关键枢纽蛋白连接了低氧应激反应和泛素化降解肿瘤抑制因子。该研究揭示了肾癌中SPOP的原癌基因功能,为SPOP作为潜在分子探针或药物靶标提供线索,同时也为肾癌诊断和治疗提供新的理论依据。
此研究得到了国家自然科学基金委、科技部、中科院等有关项目的资助。
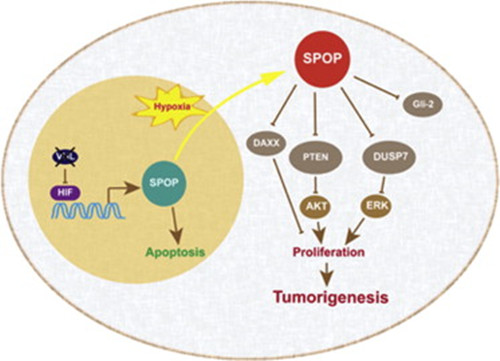
SPOP是引发肾癌产生的核心因子